中国化妆品备案注册法规操作指南
背景介绍
2020年6月29日,中国国务院正式颁布《化妆品监督管理条例》(Cosmetics Supervision and Administration Regulation, CSAR,国令第727号),并于2021年1月1日正式实施。这一法规的出台标志着中国化妆品监管体系迈入全新的发展阶段,确立了以安全性和科学监管为核心的现代化管理体系。
作为中国化妆品行业的核心法规,CSAR 在产品分类、注册备案要求、生产经营管理、原料管理、功效宣称、标签标识、监督检查及法律责任等方面进行了全面而系统的改革。新法规强化了企业主体责任,要求化妆品注册人、备案人及生产企业建立健全的产品质量和安全管理体系,确保产品的安全性和合规性。此外,CSAR 引入了风险管理原则、原料安全评估制度,并对产品功效宣称提出了更加严格的科学验证要求,以提升消费者权益保护水平。
在 CSAR 框架下,中国国家药品监督管理局(NMPA)陆续发布了一系列配套法规和技术规范,包括《化妆品分类规则和分类目录》《化妆品注册备案管理办法》《化妆品标签管理办法》《化妆品功效宣称评价规范》《化妆品注册备案资料管理规定》等,进一步细化了监管要求,确保法规的有效落地实施。这些法规的出台不仅提高了化妆品行业的准入门槛,也推动了行业向更加科学化、透明化和国际化的方向发展。
本指南旨在帮助化妆品企业全面理解并严格遵循 CSAR 及其配套法规的要求,确保产品在中国市场的合规性与安全性,同时降低合规风险,提升市场竞争力,推动行业健康、可持续发展。
化妆品定义
“化妆品,是指以涂擦、喷洒或者其他类似方式,涂抹于皮肤、毛发、指甲、口唇等人体表面,以清洁、保护、美化、修饰为目的的日用化学工业产品。”(《化妆品监督管理条例》第一章第三条)
化妆品分类
化妆品分为特殊化妆品和普通化妆品。国家对特殊化妆品实行注册管理,对普通化妆品实行备案管理。(《化妆品监督管理条例》第一章第四条)
染发、烫发、祛斑美白、防晒、防脱发的化妆品以及宣称新功效的化妆品为特殊化妆品。
特殊化妆品以外的化妆品为普通化妆品。
香皂不适用本条例,但是宣称具有特殊化妆品功效的适用本条例。(《化妆品监督管理条例》第六章第七十七条)
用于育发、脱毛、美乳、健美、除臭的化妆品自本条例施行之日起设置5年过渡期,过渡期内可以继续生产、进口、销售,过渡期满后不得生产、进口、销售该化妆品。(《化妆品监督管理条例》第六章第七十八条)
化妆品的监管部门
中国化妆品的监管部门主要包括以下几个主体:
国家药品监督管理局(NMPA):主要职责包括制定相关法规、政策和标准;特殊化妆品上市前审核;化妆品上市后的风险管理;产品抽检;飞行检查等。
国家药品食品检定研究院(NIFDC):主要职责包括制定技术标准和检测方法;承担化妆品上市前注册的技术审评工作等。
地方药品监督管理部门(Local MPAs):主要职责包括化妆品备案管理(上市前备案);承担化妆品生产的行政许可;产品抽检;开展不良反应监测、评估及处理等。
国家/地方市场监督管理局(State/Local AMR):主要职责包括综合市场监管与管理;市场主体的统一登记注册;监督和管理市场秩序等。
国家药品不良反应监测中心(NCADRM):主要职责包括化妆品不良反应监测与上市后安全性评估;制定相关技术标准等。
化妆品在中国市场上市要求(一般贸易)
化妆品在中国市场上市,主要有一般贸易和线上渠道两种方式。针对一般贸易渠道,监管要求和准入流程具体如下。
1. 化妆品上市流程
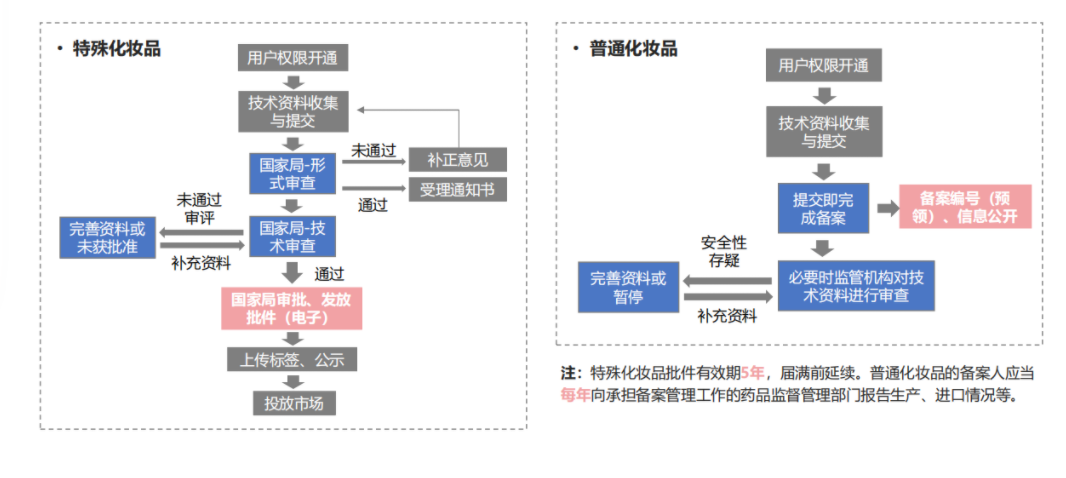
化妆品分为特殊化妆品和普通化妆品,特殊化妆品为注册管理,普通化妆品为备案管理。不同类别的产品有不同的审批流程。
普通化妆品
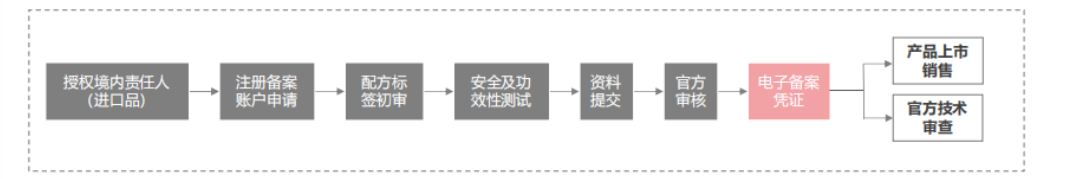
特殊化妆品
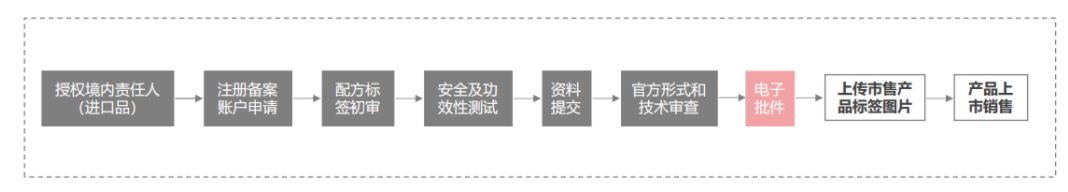
2. 化妆品注册人、备案人、境内责任人职责与资质要求
2.1 注册人/备案人
注册人/备案人:规定获得了特殊化妆品注册证的注册人或通过化妆品备案的备案人,以自己的名义将产品投放市场,并对产品全生命周期质量安全和功效宣称负责。
条件:
依法设立的企业或者其他组织;
有与申请注册、进行备案的产品相适应的质量管理体系;
有化妆品不良反应监测与评价能力。
化妆品注册人、备案人和受托生产企业应当设立质量安全负责人,该负责人应具备与化妆品质量安全相关的专业知识,并具有5年以上化妆品生产或质量安全管理经验。
2.2 境内责任人
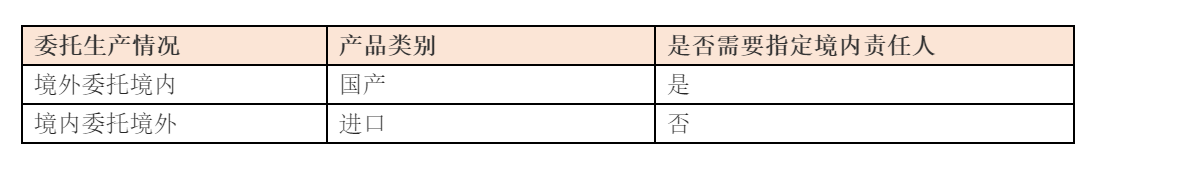
注册人、备案人在境外的,应当指定我国境内的企业法人作为境内责任人。
义务:
以注册人、备案人的名义,办理化妆品注册、备案;
协助注册人、备案人开展化妆品不良反应监测;
协助注册人、备案人实施化妆品召回工作;
按照与注册人、备案人的协议,对投放境内市场的化妆品承担相应的质量安全责任
配合药品监督管理部门的监督检查工作。
3. 化妆品注册备案资料要求
3.1 化妆品注册备案资料概览
根据《化妆品注册备案资料管理规定》,注册人、备案人办理注册或者备案时,应当提交以下资料:
《化妆品注册备案信息表》及相关资料:产品名称、企业信息、分类编码、已上市证明等
产品名称信息
产品配方
产品执行的标准
产品标签样稿
产品检验报告
产品安全评估资料
根据《化妆品监督管理条例》(CSAR)及其配套法规要求,自2022年1月1日起,所有在中国市场销售的普通化妆品和特殊化妆品,如果有功效宣称(如“美白”、“保湿”、“抗皱”等),企业必须提供功效宣称依据摘要,并上传至国家药品监督管理局(NMPA)指定的专门网站,供公众查询。
3.2 产品配方
产品配方包括原料序号、原料名称、百分含量、使用目的、商标名、原料生产商及原料安全信息等。要点分析:
原料安全信息:填写产品所使用原料的生产商信息并上传由原料生产商出具的原料安全信息文件;或填写原料报送码关联原料安全信息文件。
报送码申请:主要依据《化妆品原料安全相关信息报送指南》的要求,并通过国家药品监督管理局原料安全信息服务平台进行操作。
3.3 产品执行标准
产品执行的标准包括产品名称、全成分、生产工艺、感官指标、微生物和理化指标及质量控制措施、使用方法、贮存条件、使用期限等。
3.4 产品检验报告
注册或者备案产品的产品检验报告,由化妆品注册和备案检验机构出具;依据为《化妆品安全技术规范》、《化妆品注册和备案检验工作规范》等法规规定。
3.4.1 产品检验报告包含内容
产品检验报告包括微生物与理化检验、毒理学试验、人体安全性试验报告和人体功效试验报告等。
3.4.2 豁免提交毒理学试验报告
普通化妆品的生产企业已取得所在国(地区)政府主管部门出具的生产质量管理体系相关资质认证,且产品安全风险评估结果能够充分确认产品安全性的,可免于提交该产品的毒理学试验报告,有下列情形的除外:
产品宣称婴幼儿和儿童使用的;
产品使用尚在安全监测中化妆品新原料的;
根据量化分级评分结果,备案人、境内责任人、生产企业被列为重点监管对象的。
有多个生产企业生产的,所有生产企业均已取得所在国(地区)政府主管部门出具的生产质量管理体系相关资质认证的,方可免于提交毒理学试验报告。
3.5 安全评估
化妆品注册、备案前,注册申请人、备案人应当自行或委托专业机构开展安全评估。从事安全评估的人员应当具备化妆品质量安全相关专业知识,并具有5年以上相关专业从业经历。
2025年5月1日起,化妆品注册人、备案人申请注册或进行备案时,需提交符合《化妆品安全评估技术导则(2021年版)》等文件的完整版安全评估资料。
4. 化妆品注册备案试验要求
根据《化妆品监督管理条例》和《化妆品注册备案资料管理规定》,化妆品在注册或备案时,必须进行相应的测试,以确保产品的安全性和功效宣称的真实性。
4.1 安全性测试
根据《化妆品注册和备案检验工作规范》,所有注册或备案的化妆品都必须进行安全性检测,以确保产品不会对人体健康造成危害。
包括:理化指标检测,微生物检测、毒理学测试(特定情况下的普通化妆品可免于毒理学测试)。
4.2 功效评价测试(根据功效宣称决定)
根据《化妆品功效宣称评价规范》的要求,化妆品企业在进行产品注册或备案时,如产品具有特定功效宣称(如美白、抗皱、保湿、防晒等),需要提供功效宣称的依据,并在国家药监局(NMPA)指定的专门网站上传功效宣称依据的摘要,以便公众查询和监管部门审查。
能够通过视觉、嗅觉等感官直接识别的(如清洁、卸妆、美容修饰、芳香、爽身、染发、烫发、发色护理、脱毛、除臭和辅助剃须剃毛等),或者通过简单物理遮盖、附着、摩擦等方式发生效果(如物理遮盖祛斑美白、物理方式去角质和物理方式去黑头等)且在标签上明确标识仅具物理作用的功效宣称,可免予公布产品功效宣称依据的摘要。
根据具体功效宣称选择合适的评价依据
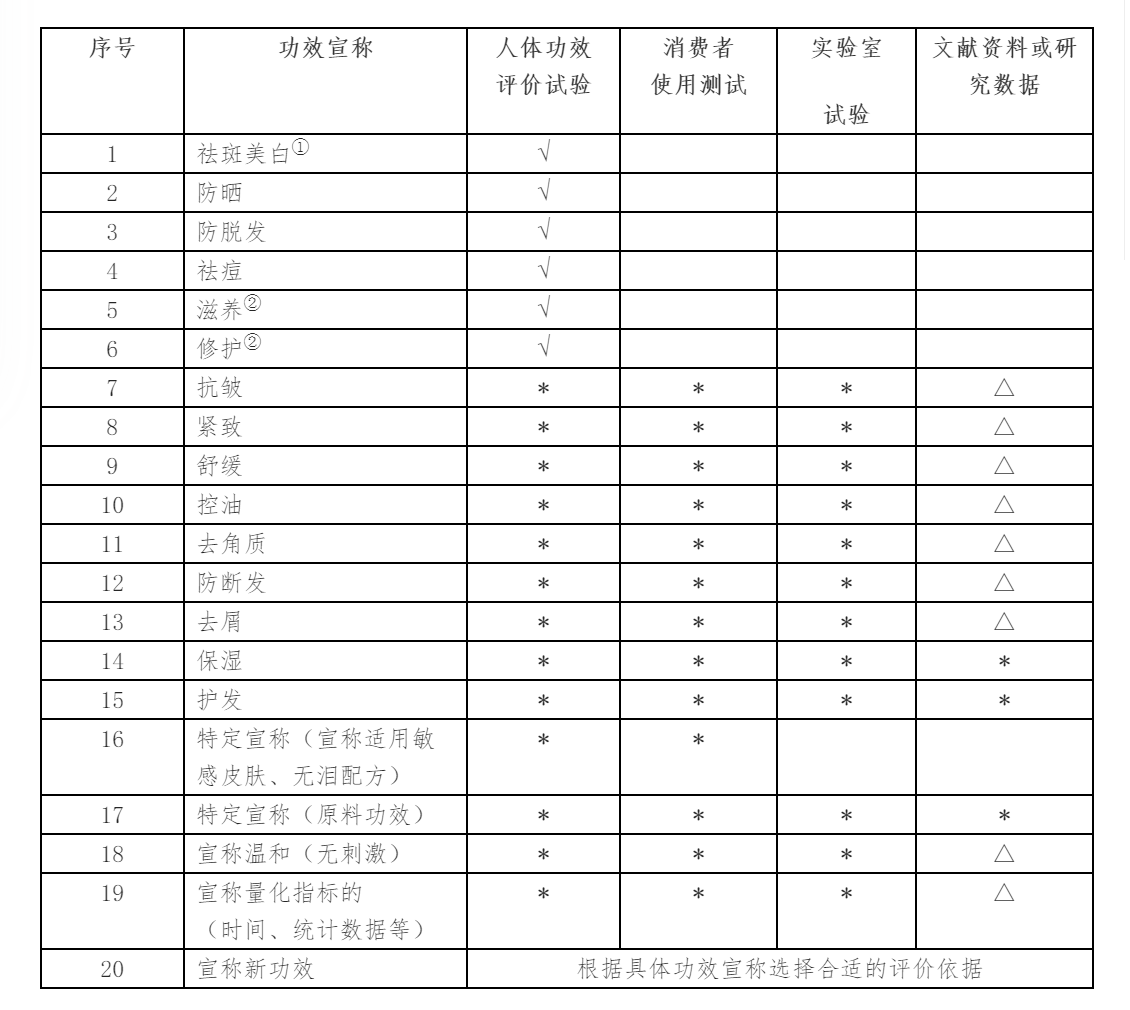
说明:
选项栏中画√的,为必做项目;
选项栏中画*的,为可选项目,但必须从中选择至少一项;
选项栏中画△的,为可搭配项目,但必须配合人体功效评价试验、消费者使用测试或者实验室试验一起使用。
注释:
① 仅通过物理遮盖作用发挥祛斑美白功效,且在标签中明示为物理作用的,可免予提交产品功效宣称评价资料;
② 如功效宣称作用部位仅为头发的,可选择体外真发进行评价。
要点分析:
微生物检验、理化检验、毒理学检验、人体安全性试验、特殊宣称(防晒、祛斑美白、防脱发、新功效)功效实验,需要在中国化妆品注册和备案检验机构进行检验。
5. 化妆品注册备案标签要求
2021年5月31日,国家药监局发布实施《化妆品标签管理办法》的公告(2021年第77号),鼓励化妆品注册人、备案人自本公告发布之日起,按照《办法》规定对化妆品进行标签标识。自2022年5月1日起,申请注册或者进行备案的化妆品,必须符合《办法》的规定和要求;此前申请注册或者进行备案的化妆品,未按照本《办法》规定进行标签标识的,化妆品注册人、备案人必须在2023年5月1日前完成产品标签的更新,使其符合《办法》的规定和要求。
5.1 化妆品标签定义
化妆品标签,是指产品销售包装上用以辨识说明产品基本信息、属性特征和安全警示等的文字、符号、数字、图案等标识,以及附有标识信息的包装容器、包装盒和说明书。化妆品注册人、备案人对化妆品标签的合法性、真实性、完整性、准确性和一致性负责。
注意:化妆品的最小销售单元应当有标签。
注意:除文字内容外,标签中的符号、数字、图案等标识也属于化妆品标签上的内容,使用其他文字或者符号的,应当在产品销售包装可视面使用规范汉字对应解释说明。
5.2 必须标注的内容
(一)产品中文名称、特殊化妆品注册证书编号
(二)注册人、备案人的名称、地址,注册人或者备案人为境外企业的,应当同时标注境内责任人的名称、地址
(三)生产企业的名称、地址,国产化妆品应当同时标注生产企业生产许可证编号
(四)产品执行的标准编号
(五)全成分
在销售包装可视面标注化妆品全部成分的原料标准中文名称,以“成分”作为引导语引出,并按照各成分在产品配方中含量的降序列出。配方中存在含量不超过0.1%(w/w)的成分的,所有不超过0.1%(w/w)的成分应当以“其他微量成分”作为引导语引出另行标注,可以不按照成分含量的降序列出。
注意:其他微量成分包含原料含量等于0.1%(w/w)的成分。
(六)净含量
(七)使用期限
形式1:生产日期和保质期
形式2:生产批号和限期使用日期。
① 具有包装盒的产品,在直接接触内容物的包装容器上标注使用期限时,除可以选择上述方式标注外,还可采用直接标注生产批号和开封后使用期限的方式。
②具有包装盒的产品,还应当同时在直接接触内容物的包装容器上标注产品中文名称和使用期限。
(八)使用方法
(九)必要的安全警示用语
(十)法律、行政法规和强制性国家标准规定应当标注的其他内容。
化妆品加贴中文标签的(如进口化妆品上市时),中文标签有关产品安全、功效宣称的内容需与原标签相关内容对应一致。即产品在中国上市时宣称的关于安全、功效的宣称与在原产国销售时保持一致。
6. 化妆品注册备案周期
6.1 化妆品注册备案流程
根据《化妆品注册备案管理办法》,国家对特殊化妆品实行注册管理,对普通化妆品实行备案管理。
6.2 化妆品注册备案周期

*实际周期根据具体产品类型、测试以及多方资料搜集情况有关。
7. 化妆品注册备案变更及延续
7.1 化妆品注册备案变更
根据《化妆品注册备案资料管理规定》,已注册产品的注册事项发生变更的,应当在拟变更产品生产或者进口前提交相应资料,完成相应的变更之后,方可生产或者进口。已备案产品的备案事项发生变更的,应当在拟变更产品上市或者进口前提交相应资料,完成相应的变更之后,方可上市或者进口。变更前已生产、上市或者进口的产品可以销售至保质期结束。所涉及的变更类型包括:
注册人、备案人、境内责任人或者生产企业的名称、住所等变更(生产场地未改变)
已注册或者备案产品的产品名称变更
生产场地变更
已注册或者备案产品所使用原料的生产商、原料质量规格变更
产品执行标准变更
产品标签样稿变更
产品安全评估资料内容变更
产品分类变更
注册人变更
变更境内责任人
涉及其他事项变更的,应当提交拟变更事项的情况说明,并根据具体情况提交相关资料。
7.2 化妆品注册备案延续
根据《化妆品注册备案管理办法》,特殊化妆品注册证有效期届满需要延续的,注册人应当在产品注册证有效期届满前90个工作日至30个工作日期间提出延续注册申请,并承诺符合强制性国家标准、技术规范的要求。注册人应当对提交资料和作出承诺的真实性、合法性负责。逾期未提出延续注册申请的,不再受理其延续注册申请。
根据《化妆品注册备案资料管理规定》,申请特殊化妆品注册证有效期延续的,应当提交以下资料:
注册延续申请表
产品自查情况说明
根据现行法规、标准调整情况,应当提交相应的产品检验报告
8. 化妆品上市后监管要求
化妆品在完成注册或备案并上市销售后,仍需接受国家药品监督管理局(NMPA)及地方监管部门的持续监管,以确保产品的安全性、功效真实性及合规性。
2022年1月1日起,普通化妆品统一实施年度报告制度。备案人应当于每年1月1日至3月31日期间,通过注册备案平台,提交备案时间满一年普通化妆品的年度报告。
8.1 产品质量安全监管
根据《化妆品监督管理条例》、《化妆品生产经营监督管理办法》以及《化妆品安全技术规范》等,监管部门会定期对市场上的化妆品进行随机抽样检测,确保产品符合国家标准。
8.2 不良反应监测
根据《化妆品不良反应监测管理办法》,建立化妆品不良反应监测系统,收集消费者反馈。国家药监局定期发布化妆品不良反应监测报告。若某款产品存在严重安全隐患,可能要求企业召回或停售。化妆品注册人、备案人应当监测其上市销售化妆品的不良反应,及时开展评价,按照国务院药品监督管理部门的规定向化妆品不良反应监测机构报告。受托生产企业、化妆品经营者和医疗机构发现可能与使用化妆品有关的不良反应的,应当报告化妆品不良反应监测机构。
化妆品在中国市场上市要求(线上渠道)
在中国市场,化妆品也可以通过线上渠道进行上市销售。其中,线上渠道主要包括:国内电商平台和跨境电商(CBEC,Cross-Border E-Commerce)。
1. 国内电商平台销售化妆品的监管要求
适用于已完成注册或备案的国产或进口化妆品,通过国内电商平台销售。电商平台需审核商家资质,确保所售产品已完成注册或备案。平台需建立投诉举报机制,配合监管部门处理违规商品。同时,产品必须使用中文标签,并符合《化妆品标签管理办法》,禁止虚假宣传。
2. 跨境电商(CBEC)销售化妆品的监管要求
适用于未在中国境内注册或备案的进口化妆品。通过跨境电商零售进口模式进入中国市场,消费者在跨境电商平台上下单,商品通过保税仓发货或海外直邮方式交付。跨境电商模式通过简化备案和检验流程为海外化妆品提供了快速进入中国市场的路径,但同时也受限于正面清单、销售渠道等。
2.1 化妆品准入要求
与一般贸易中所有进口的化妆品都需要完成国家药监局(NMPA)注册或备案相比,通过跨境电商进口的化妆品无需国内注册或备案,但需要符合中国《跨境电商零售进口商品清单》(正面清单)和成分安全要求。
根据商务部财务司发布的《关于完善跨境电子商务零售进口监管有关工作的通知》,跨境电商零售进口商品按“个人自用”监管,不执行有关商品首次进口许可批件、注册或备案要求,但需符合正面清单。
中国《跨境电商零售进口商品清单》(正面清单):仅允许清单内化妆品通过跨境电商进口。
2.2 标签
产品标签需符合《化妆品监督管理条例》《化妆品标签管理办法》等法规要求,确保标签信息真实、完整、规范。线上销售的化妆品还需符合《电子商务法》要求,确保标签信息与备案一致。
2.3 消费者“个人自用”限制
通过跨境电商购买的化妆品仅限个人使用,不得用于二次销售。购买人需进行实名认证,并符合跨境电商年度购买额度(26,000元人民币/人)。
我们的服务
中国化妆品注册备案
中国化妆品新原料注册备案
中国化妆品原料安全信息报送码申请
中国化妆品安全与功效检测
毒理安全评估
配方/标签/原料审核
境内责任人
上述信息,涵盖图片、视频以及各类文字资料,美天彩仅扮演信息存储的角色。若存在任何侵犯知识产权或其他合法权益的情形,请立即联系我们删除,切实维护您的权益。
郑重声明
- 延伸阅读:
- 上一篇:化妆品安全风险监测与评价标准规定解读
- 下一篇:中国化妆品新原料注册备案指南

Experts Q & A
外贸专家答疑
为了帮助您更快地解决问题,建议向我们的外贸专家进行咨询,提供专业的方案咨询和策划。


马上留言 (0) 0